众所周知,中枢神经系统的神经细胞一旦受到损伤则难以恢复,这是一个不可逆的过程。帕金森是一种缓慢发生的选择性中脑黑质多巴胺能神经元丧失和纹状体多巴胺含量明显减少的神经系统退行性疾病。
正常情况下,黑质中的多巴胺神经元利用酪氨酸羟化酶将左旋酪氨酸转化为左旋多巴,再经过脱羧酶的作用转化为多巴胺。作为神经递质的多巴胺经黑质-纹状体束转运至纹状体的尾状核和壳核细胞,传递信号。多巴胺的缺乏导致锥体外系功能失调,从而出现静止性震颤、肌僵直、动作减少及平衡障碍等临床表现。帕金森病在65岁以上的老年人口中约为1%。
传统观点认为,中枢神经系统的神经细胞是一种终末细胞,创伤、中毒、缺血缺氧等病理过程引起的神经元丢失是一个不可逆的过程,因此寻求一种从病因上提高神经系统细胞数目的治疗具有重要意义。
干细胞治疗的优势
与现有的医疗和手术治疗的帕金森病相比,干细胞疗法代表一种进步的治疗方案,已成为临床上具有竞争力的新疗法,现有研究表明其能促使长期持久地,大幅改善运动障碍,阻断疾病进程。
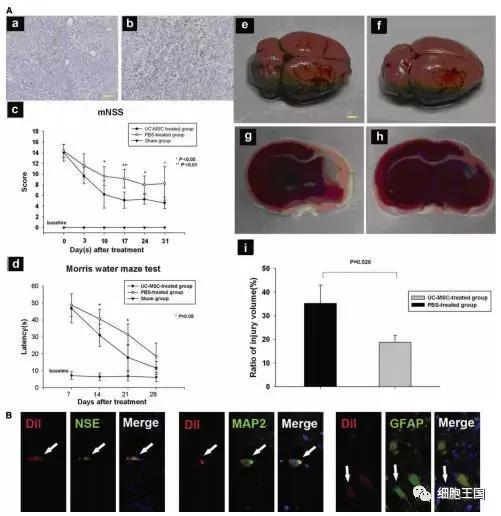
《BASIC AND EXPERIMENTAL RESEARCH基础与实验研究杂志》曾发表过一篇研究,研究人员使用(MSC)间充质干细胞移植治疗脑梗死模型大鼠并观察疗效,结果发现移植的MSC能显著减少梗死面积并促进大鼠神经功能的恢复,还发现MSC能整合到大鼠大脑的脉管系统,部分能分化为内皮细胞,治疗组大鼠梗死侧大脑血管密度、血管内皮生长因子和碱性成纤维细胞生长因子表达水平显著增加。(见图1-2)
图1:(UC-MSC)脐带间充质干细胞体在内神经分化,及治疗后神经功能的改善
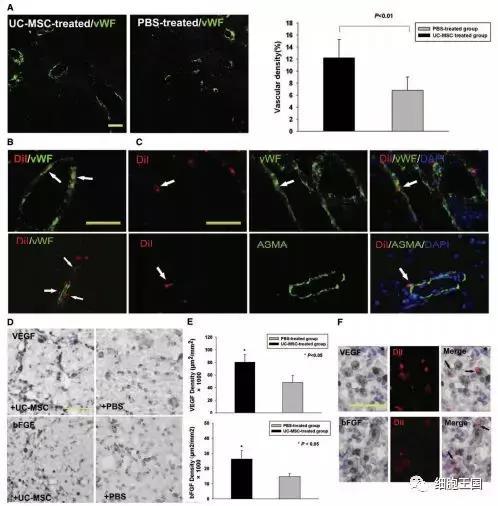
图2:(UC-MSC)脐带间充质干细胞可增加血管密度和血管生成因子的表达。
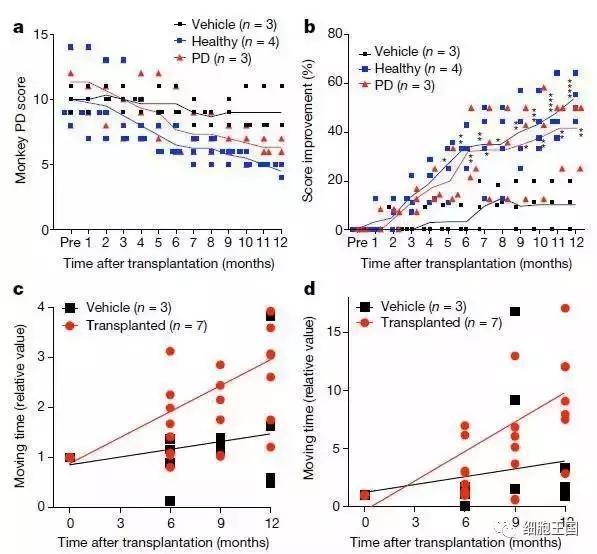
2017年8月30日,发表于Nature期刊上的一项研究中,日本科学家将由人类诱导多能干细胞(iPS)制成的神经元移植到帕金森病猴子中,使它们在两年内症状得到显著改善,并且没有产生任何危险的副作用。
在这项研究中,Takahashi的团队将健康人群和帕金森患者的iPS细胞转化为能产生多巴胺的神经元。然后将这些细胞移植到猕猴帕金森模型中。移植的脑细胞存活了至少两年,并与猴子的脑细胞形成了连接,被细胞治疗的猴子运动能力得到显著改善。
猴子的行为分析。图片来源:Nature
2008年北京和众华信治疗中心应用脐带间充质干细胞(UC-MSC)进行鞘内注射移植治疗帕金森病患者30例,采用帕金森病统一评分量表对患者移植前后神经功能进行评定,30例患者移植后3个月帕金森病统一评分量表分值均明显降低 (P<0.01),患者震颤、强直、运动迟缓、姿势不稳等临床症状均得到明显改善,均未出现移植物抗宿主病。
2010年~2012年江西省人民医院神经内科收治的帕金森病患者32例,患者进行自体骨髓干细胞移植后 1、3个月的UPDRS评分较移植前均明显降低,其中运动功能和日常生活能力明显改善,移植术后1、3、6个月临床症状的改善率分别为71.9%、78.1%和31.3%。
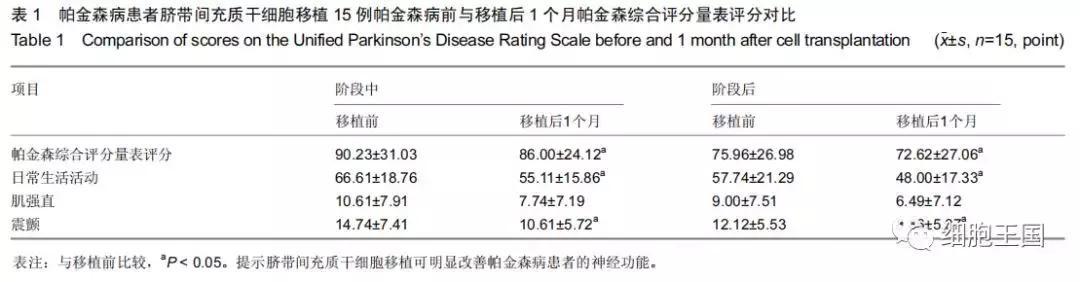
河南新乡医学院第三附属医院神经内二科采取脐带间充质干细胞移植治疗15例帕金森病患者,患者平均年龄63.4岁,干细胞治疗后结合扩张血管、抗自由基、营养神经、稳定细胞膜等常规治疗。分别于干细胞移植前和移植后1个月,采用帕金森病综合评分量表对患者进行评定,主要从4个方面进行了评价,包括了42个项目:①第1部分:精神、行为和情绪。②第2部分:日常活动。③第3部分:运动功能。④第4部分:治疗的并发症。(分值越高表示神经功能缺损越严重。)
海军总医院全军神经外科中心将5~11周人胚胎的前脑细胞在体外稳定扩增 ,并向多巴胺神经元转化,通过立体定向手术将其植入50例帕金森患者的纹状体移植手术后随访8~30个 月 (平均24个月 ),有效率为92,证实应用体外长期扩增的人类神经干细胞移植治疗帕金森是可行和有效的。
展望
自20世纪70年代末至今,不同类型的干细胞已被用于多种疾病的治疗,包括免疫疾病、神经疾病、心血管疾病,以及消化疾病和内分泌疾病的治疗。目前MSCs移植治疗PD较为认可的作用机制主要有MSCs移植可定向分化替代变性或缺失的多巴胺能神经元,也可分泌多种生物活性因子,起神经营养、抗细胞凋亡、微血管再生、免疫调控和抗炎效应; 此外,还可调节细胞代谢保护多巴胺能神经元。当然,更多其它潜在的作用机制尚需大量实验和前期临床试验研究进一步探索、证实。总之,干细胞移植治疗帕金森的上述作用机制并非相互独立,而是相互依赖,相互影响,共同营养、修复和促进受损多巴胺能神经元再生,进而提高多巴胺递质分泌水平,从病理基础上阻止或逆转黑质-纹状体通路进行性退变,改善运动障碍。
干细胞治疗疾病是未来行业内的大趋势,在科学技术不断提高的情况下,相信干细胞应用将更加广阔。