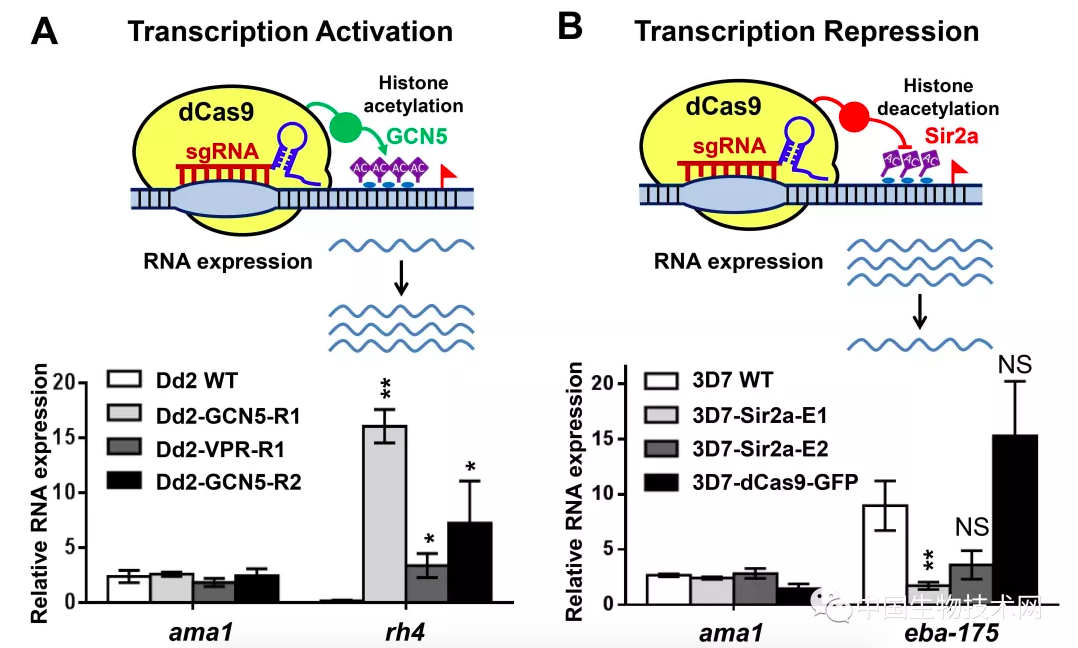
图A: CRISPR/dCas9-GCN5 系统激活基因表达示意图与激活恶性疟原虫Rh4基因表达
图B: CRISPR/dCas9-Sir2a系统抑制基因表达示意图与抑制恶性疟原虫Eba-175基因表达。
近日,来自上海斯巴德研究所江陆斌研究组在国际学术期刊《PNAS》发表了一项新研究。研究内容是利用CRISPR/dCas9系统,在恶性疟原虫中成功构建了基于表观遗传修饰的新型基因编辑工具。
疟疾与艾滋病、结核病一起被列为全球三大传染性疾病。疟原虫是引起疟疾的真核病原微生物,其中恶性疟原虫的感染致死率最高。分子水平的遗传操作是研究恶性疟原虫病理学以及抗药机制的重要工具。然而,疟原虫中通过同源重组机制进行基因修饰的效率极低,而且恶性疟原虫缺乏可运行RNAi机制的关键原件,因而对疟原虫的研究急需发展一种高效简便的基因编辑工具。
江陆斌研究团队研究出的新型遗传操作工具可以分别将dCas9与恶性疟原虫乙酰转移酶(PfGCN5)和去乙酰化酶 (PfSir2a)融合表达。在特异性sgRNA 的引导下,dCas9重组蛋白可以在靶基因的转录起始位点(TSS)附近特异性调节染色质组蛋白乙酰化修饰水平,从而控制该基因表达的沉默或激活。运用此新型CRISPR/dCas9技术,该团队分别对恶性疟原虫感染人体红细胞的两个关键基因PfRh4和PfEBA-175成功地进行了表达调控,并诱导出相应的感染表型的变化。在此基础上,该团队进一步鉴定出恶性疟原虫生长必需基因PfSET1参与调节恶性疟原虫红内期生长过程的分子基础。
该研究成果为恶性疟原虫基因编辑提供了新的有效的遗传操作工具,为恶性疟原虫功能基因组学研究提供了强大的遗传操作系统。
随着我国对基因编辑的重视,越来越多的科研项目得到扶持,相信在不远的未来,国家会制定有利于基因编辑研究成果转化的相关政策,加速推动基因编辑技术用于重大疾病治疗的研究。